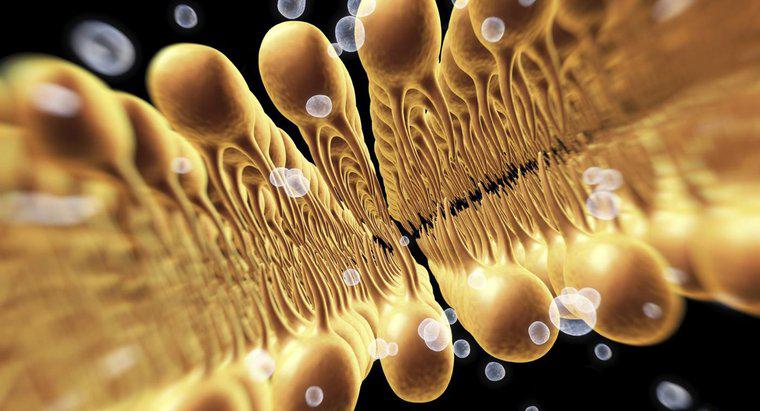
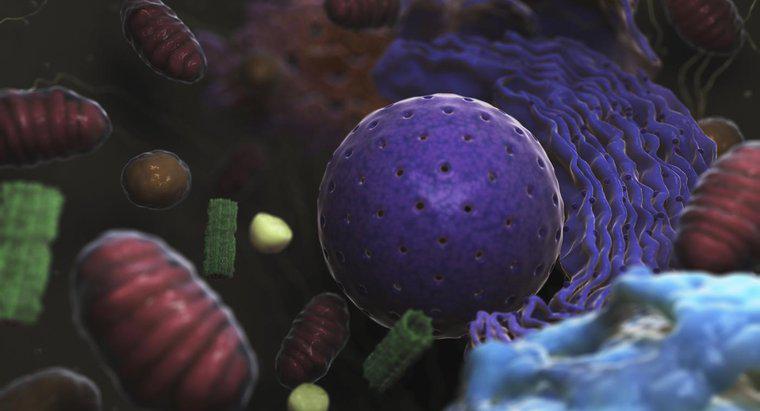
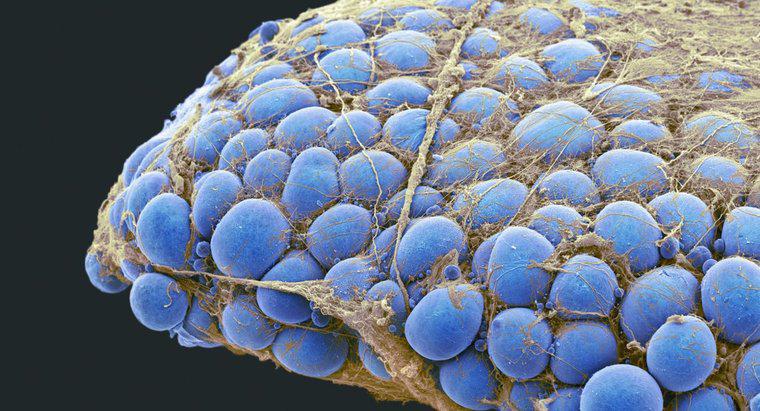
Cuando se agrupan por forma o enrejado, los siete tipos de cristales son cúbicos o isométricos, ortorrómbicos, tetragonales, hexagonales, trigonales, triclínicos y monoclínicos. Los cristales también se agrupan por sus propiedades físicas y químicas.
Las formas de los cristales son distintas pero difíciles de imaginar hasta que se ven. Además, los nombres pueden ser engañosos. Por ejemplo, un cristal cúbico no siempre tiene forma de cubo. Solo dentro de la clasificación isométrica, puede haber formas de cubos, octaedros (ocho caras) y dodecaedros (10 caras). La mayoría de las clases y formas son simétricas, pero la clase triclínica suele ser asimétrica, lo que hace que algunas formas de cristal sean extrañas.
Las propiedades químicas que se utilizan para agrupar cristales incluyen covalente, metálico, iónico y molecular. Hay diferencias distintivas en cada uno de estos. Por ejemplo, un cristal covalente tiene enlaces entre todos los átomos en el cristal, como una molécula grande, pero un cristal molecular está formado por muchas moléculas en un gran bulto. Los cristales iónicos tienen enlaces entre todos los átomos similares a un cristal covalente, pero los cristales iónicos tienen enlaces de una naturaleza más electrostática. Esto hace que sus puntos de fusión sean mucho más altos que los cristales covalentes. Los cristales metálicos tienen átomos de metal en obras de celosía específicas, pero los átomos de metal externos están libres para moverse.