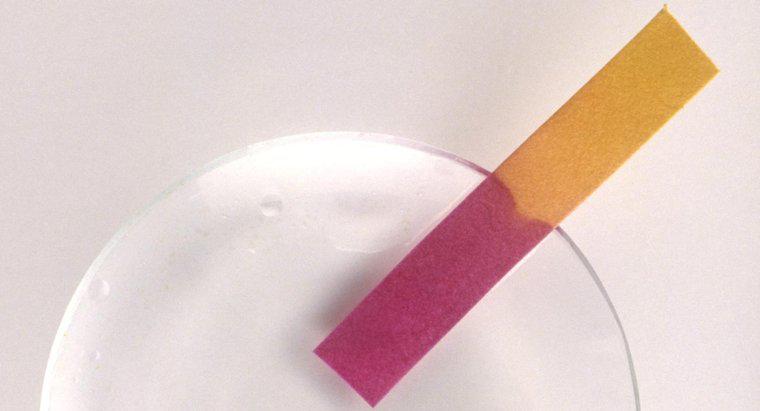Físicamente, los ácidos tienen un sabor agrio, son solubles en agua, se vuelven rojos, son corrosivos, tienen valores de pH inferiores a 7 y conducen electricidad. Estas propiedades físicas de los ácidos son un subproducto De las propiedades químicas de los ácidos. Los ácidos pueden ser soluciones o sustancias puras y pueden ser de naturaleza sólida, líquida o gaseosa.
Los ácidos se definen como sustancias que aumentan la concentración de átomos de hidrógeno, o más precisamente, átomos de hidronio (H30), en el agua. Esta ionización del ácido, que es típica de todas las sales, es la razón por la cual los ácidos conducen la electricidad. Los valores de pH se definen como el logaritmo negativo de la concentración de átomos de hidronio en una solución; por lo tanto, los ácidos dan un valor de pH inferior a 7 porque las concentraciones de hidronio son mayores que 10 ^ -7 moles por litro. La fuerza de un ácido, y por lo tanto su corrosividad, está determinada por la cantidad de ácido que se ioniza, o se disocia, en átomos de hidronio en agua, con ácidos fuertes que se disocian completamente y ácidos débiles solo parcialmente. Estos átomos de hidronio reaccionan químicamente con metales y tejidos vivos. Esta propiedad corrosiva es útil en el cuerpo humano, ya que el ácido en el estómago ayuda en la digestión de los alimentos. Los ácidos débiles también se usan como aditivos en los alimentos para infundir un sabor agrio.