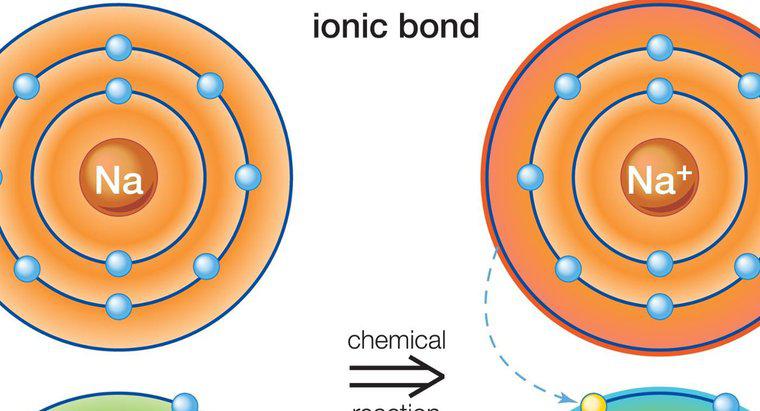
El nombramiento de compuestos iónicos requiere la identificación correcta de las especies de cationes y aniones presentes. En ciertos casos, la carga del ion es importante para una denominación precisa.
Los principios de nomenclatura química estándar identifican primero el catión en el nombre y el segundo anión. En los compuestos iónicos, el catión es típicamente un metal, y la primera parte del nombre del compuesto es simplemente ese metal. Si el catión puede existir naturalmente en múltiples estados cargados, la carga del metal, también conocida como la valencia, debe identificarse en el nombre del compuesto con números romanos. Por ejemplo, el hierro puede existir en el estado positivo de dos o tres de carga positiva. Estos se denominarían hierro (II) y hierro (III), respectivamente.
El paso final para nombrar un compuesto iónico es identificar correctamente el anión que está presente. Los aniones pueden ser un solo ion, como el bromuro, o moléculas complejas que están formadas por múltiples átomos, como el sulfato. Para estos aniones complejos, los parámetros de denominación adicionales están en su lugar. Los elementos que son capaces de formar múltiples oxianiones, como el nitrógeno y el azufre, tienen una terminación de -ite o de -ate, dependiendo del número de moléculas de oxígeno presentes. Un ejemplo de un compuesto iónico debidamente nombrado es el sulfato de hierro (II) para la fórmula iónica Fe (SO4).