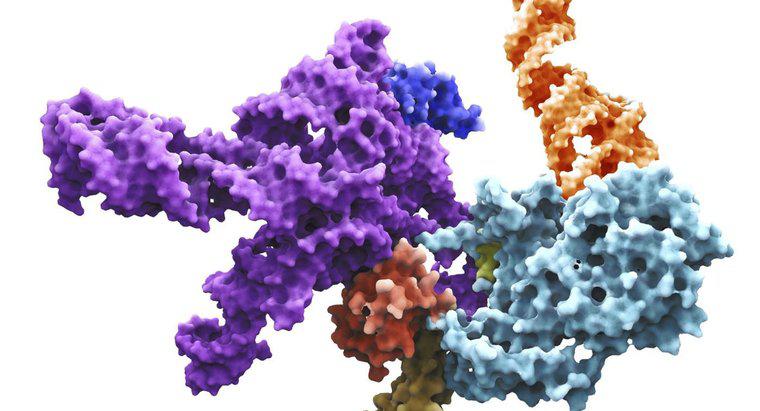
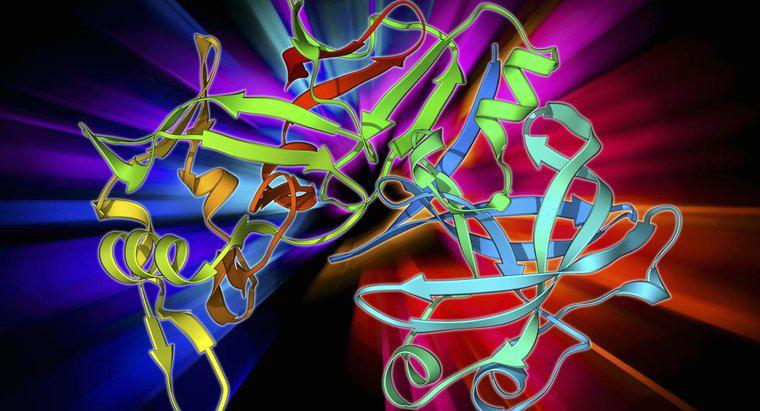
Las enzimas en ebullición elevan su temperatura, lo que aumenta la velocidad de actividad de las enzimas. Sin embargo, existe un límite a partir del cual las enzimas dejan de funcionar y se desnaturalizan. Demasiado calor rompe los enlaces químicos que mantienen unidas a las enzimas.
El aumento de la temperatura aumenta la colisión entre las moléculas de sustrato y las moléculas de agua. La velocidad del movimiento molecular aleatorio y la energía de vibración de las moléculas aumenta con un aumento de la temperatura. Las enzimas consisten en aminoácidos individuales unidos en una estructura tridimensional por enlaces químicos entre aminoácidos. Cuando las temperaturas aumentan más allá de un límite superior, las enzimas pierden la estructura tridimensional, lo que las hace incapaces de adaptarse a sus moléculas de sustrato objetivo.
En consecuencia, las enzimas se desnaturalizan y dejan de funcionar. Este es un proceso irreversible, y bajar la temperatura no restaura las funciones de las enzimas. Por otro lado, las bajas temperaturas retardan las actividades de las enzimas. En el punto de congelación, el movimiento molecular disminuye considerablemente debido a la formación de sólidos, lo que hace que las moléculas se enganchen en una estructura cristalina rígida.
Las enzimasson proteínas tridimensionales que catalizan las reacciones químicas. Sin enzimas, algunas reacciones no tendrían lugar o serían demasiado lentas para sostener la vida. En otras palabras, las enzimas facilitan la formación o ruptura de los enlaces atómicos. La velocidad a la que las enzimas afectan sus reacciones respectivas y la capacidad de conservar su estructura depende en gran medida de la temperatura.